Hydrogène, propriétés physico-chimiques & défis technologiques
Décryptage signé Alexandre Fleurentin, expert technique et judiciaire (Métallo Corner Conseils).
Constitué d’un proton et d’un électron, l’atome d’hydrogène est l’élément le plus petit du tableau de classification des éléments chimiques (Mendeleïev). Deux atomes d’hydrogène forment la molécule dihydrogène (H2).
Ce gaz n’existe quasiment pas à l’état naturel, il peut être produit par vaporeformage du méthane, par l’oxydation partielle du pétrole, par gazéification du charbon et dans une moindre mesure par l’électrolyse de l’eau.
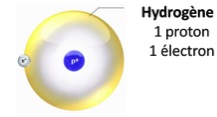
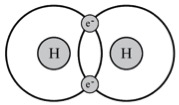
Figure 1 : Représentation de l’atome d’hydrogène et de la molécule de dihydrogène
De leurs propriétés physico-chimiques découlent les avantages et les inconvénients de leurs utilisations, principal enjeu de demain en vue de favoriser le développement d’énergies renouvelables dans la production d’électricité et limiter de ce fait les émissions de gaz à effet de serre.
Comprendre les propriétés de ce gaz permet d’identifier les défis technologiques d’aujourd’hui et de demain.
Densité et mobilité
Le dihydrogène est le plus léger des gaz, il se trouve à l’état gazeux à la température ambiante et se liquéfie à -253°C (cryogénie). Le fort pouvoir diffusif du dihydrogène nécessite par contre une mise en pression de ce gaz ou une liquéfaction de celui-ci si l’on souhaite le transporter. Ces deux solutions occasionnent une dépense énergétique supplémentaire.
Aussi bien à l’état liquide que gazeux, le dihydrogène est particulièrement sensible aux fuites à cause de la faible viscosité et de sa faible masse molaire. Par conséquent, un système qui serait étanche à l’air ou à tout autre gaz peut s’avérer inefficace face au dihydrogène.
Il est intéressant de rappeler que les éléments des installations industrielles travaillant sous H2, à l‘image des joints d’étanchéités, des vannes, des soupapes, des valves, des flexibles, des clapets anti-retour, des robinets, des compresseurs devront être conçus en intégrant cette forte mobilité tout en disposant d’un système de détection adapté face à d’éventuelles fuites.
Cette mobilité importante peut être perçue comme positif au niveau de la sécurité des installations dans la mesure où cela tendra à limiter le confinement de l’H2 et d’éviter de se retrouver dans les plages du domaine d’inflammabilité (Cf. figure 2) en présence d’un comburant.
De l’inflammabilité à la détonation
Dans l’inconscient collectif, travailler sous dihydrogène reste angoissant probablement suite à l’incendie du zeppelin Hindenburg (Cf. figure 2) après sa 10ème traversée de l’Atlantique dans le New Jersey (1937), à l’utilisation de la « bombe H » utilisée pendant la 2ème guerre mondiale sur les villes d’Hiroshima et de Nagasaki (1945) ou à l’explosion des réservoirs de la navette spatiale américaine Challenger (1986).

Figure 2 : Incendie du zeppelin Hindenburg à Lakehurst à l’approche de son mât d’amarrage. (Source : Wikipédia)
Cette perception est loin d’être usurpée compte tenu des vastes domaines d’inflammabilité, de détonation et de sa très faible énergie d’activation ou d’auto-inflammation (Cf. Figure 3 et tableau 1). En effet, un échauffement thermique localisé, une étincelle d’ordre mécanique, l’électricité statique, … suffisent pour activer la combustion du gaz H2. On peut également ajouter que ce gaz est inodore ce qui le rend difficilement détectable sans la mise en place de technologies adaptées.
En revanche, sa flamme incolore est un avantage en cas d’incendie pour les objets environnant, puisque le phénomène de transfert thermique par rayonnement est quasi inexistant.
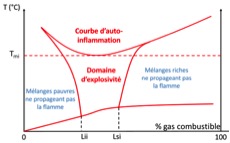
Figure 3 : Domaine d’inflammabilité

La gestion de la sécurité en milieu dihydrogène repose sur le fait de travailler autant que possible en milieu aéré (non confiné) ou d’utiliser des quantités réduites de dihydrogène tout en s’assurant du respect des règles dictées par la directive ATEX et autres normes européennes :
- NF EN M58-003 : Installation des systèmes mettant en œuvre l’hydrogène,
- ISO / TR 15916 : Considérations fondamentales pour la sécurité des systèmes hydrogénés.
La réflexion associée à la sécurité d’un système évoluant sous dihydrogène doit également concerner l’atelier ou les locaux qui abritent les installations (système de ventilation approprié, mise en place de détecteurs,..) et le personnel qui aura la charge de ces installations (maintenance préventive, formation adaptée à ce nouvel environnement de travail).
Le défis d’aujourd’hui et de demain en termes de sécurité face aux installations travaillant sous hydrogène est la mise en place de mesures préventives et protectrices afin de réduire l’occurrence des incidents. Le risque zéro n’existant pas, il faudra également limiter les conséquences dommageables face aux accidents.
L’hydrogène et les matériaux métalliques
Comme nous avons pu le constater dans les précédents chapitres, il est donc primordial d’anticiper et de maitriser le régime de combustion de l’hydrogène ainsi que les risques de fuite. Pour cela, il est nécessaire d’avoir une approche industrielle à la fois sur les systèmes mécaniques travaillant sous dihydrogène (limitation des volumes explosibles, cloisonnement avec d’éventuels comburants, calcul des taux de fuite maximal admissible, …) mais sur la compatibilité et la durabilité des matériaux utilisés avec l’hydrogène.
En ce qui concerne les matériaux métalliques, les problèmes sont d’ordre métallurgique :
- L’attaque par hydrogène avec la formation de méthane in situ dans les appareils d’équipement sous pression (bien connue dans le monde des énergies carbonées),
- De fragilisation par l’hydrogène pour les alliages à hautes caractéristiques mécaniques,
- Le clocage sous hydrogène avec la recombinaison in situ du gaz H2.
Ces phénomènes métallurgiques ont pour conséquence une impossibilité d’utiliser certains alliages en présence d’hydrogène ou d’induire une réduction drastique de la durée de vie des produits en milieu hydrogéné en accélérant les endommagements par fatigue et/ou fluage.
On peut également ajouter la grande affinité du dihydrogène avec le dichlore pour former de l’acide chlorhydrique gazeux (HCl). Cette réaction, qui peut être explosive, est catalysée par la lumière et la température. A cela, il est important d’ajouter que les matériaux métalliques à une température au-delà de 100°C dans un milieu HCl sont sujets à des problèmes de corrosion catastrophiques entrainant une durée de vie très limitée.
Pour limiter ces difficultés majeures, il existe une multitude de solutions en travaillant sur le choix des matériaux métalliques, les caractéristiques mécaniques visées, la mise en place de revêtements en effet barrière ou stockage ou en travaillant sur des systèmes de dégazage ou piégeage de l’hydrogène.
L’ensemble de ces astuces sera abordé dans de prochains articles afin de pouvoir ensemble repousser les limites de l’utilisation verte du dihydrogène.
Des solutions éprouvées existent déjà sur le marché…
Quel que soit les questions du moment concernant la mobilité / l’étanchéité ; l’inflammation / la détonation et la compatibilité métallurgique en présence d’hydrogène, il est important de se rapprocher des bonnes pratiques mises en place dans des secteurs utilisant déjà massivement le dihydrogène comme les sociétés de traitements thermiques avec leurs systèmes de régulation des traitements de nitruration, les fabricants de four industriel de recuit brillant, le secteur de la pétrochimie avec entre autre les unités de désulfuration), l’industrie nucléaire, …




COMMENTAIRES
Les bombes nucléaires qui ont frappé Nagasaki et Hiroshima étaient des bombes à fission et non pas des bombes H lesquelles sont des bombes à fusion
Hiroshima: uranium
Nagasaki: plutonium
Pas d’hydrogène…
à l’utilisation de la « bombe H » utilisée pendant la 2ème guerre mondiale sur les villes d’Hiroshima et de Nagasaki (1945)
bombe H en 1945????????????
Bien sûr pas encore de « bombe H » en 1945
’utilisation de la « bombe H » utilisée pendant la 2ème guerre mondiale sur les villes d’Hiroshima et de Nagasaki (1945)
Bombe H en 1945???